
(原标题:华东医药首个国产乌司奴单抗打针液获批上市,自免界限龙头再下一城!)
11月5日,华东医药(SZ.000963)公告称,其全资子公司杭州中好意思华东制药有限公司(以下简称“中好意思华东”)收到国度药品监督处理局(NMPA)核准签发的《药品注册文凭》,由中好意思华东汇报的乌司奴单抗打针液(赛乐信®)(研发代码:HDM3001/QX001S)的上市许可苦求取得批准,用于调理成年中重度斑块状银屑病,成为国内首个获批的乌司奴单抗生物不异药。
首个国产乌司奴单抗霸占先机,立异研发不停破损
公告领悟,赛乐信®用于斑块状银屑病的调理,是原研居品Stelara®(喜达诺®,乌司奴单抗打针液)的生物不异药,作用机理为阻断IL-12和IL-23共有的p40亚基与靶细胞名义的IL-12Rβ1受体卵白的勾通,从而扼制IL-12和IL-23介导的信号传导和细胞因子级联反馈。IL-12和IL-23是两种自然存在的细胞因子,在免疫介导的炎症性疾病中说明着枢纽作用。
Stelara®由好意思国强生公司研发,于2017年在中国获批上市,商品名为喜达诺®,当今在国内获批的相宜症有成东说念主斑块状银屑病、儿童斑块状银屑病及克罗恩病。
流行病学拜访成果领悟,中国现存跳动670万银屑病患者。斑块状银屑病约占通盘银屑病患者的80%~90%,是银屑病中最常见的类型。当今中国银屑病调理已步入生物制剂时间,相较于传总揽疗,生物制剂频频具有更优的疗效和精采的安全性。其中白细胞介素类扼制剂的疗效及安全性相对TNF-α扼制剂更有上风,如IL?12/23扼制剂、IL?17A扼制剂、IL-23p19扼制剂等。乌司奴单抗打针液给药方式为:初次45 mg皮下打针,4周后及之后每12周给以一次交流剂量,保管期一年仅需4针,是当今银屑病调理界限给药频次最低的生物制剂之一,使用便利性高,且安全性、耐受性精采、疗效合手久。寰球范围内上市16年来,乌司奴单抗打针液已在各项针对银屑病的临床考研及确凿寰宇征询中积贮了丰富的专揽教化。
赛乐信®已完成的“一项在成年中重度斑块状银屑病患者中相比QX001S打针液和乌司奴单抗打针液(喜达诺®)的有用性和安全性的多中心、速即、双盲、平行对照Ⅲ期临床征询”是国内首个针对乌司奴单抗生物不异药的大范畴临床征询,为中国东说念主群使用乌司奴单抗打针液进一步提供了丰富的临床根据及教化。
值得一提的是,中国银屑病药物阛阓范畴正在快速增长。据弗若斯特沙利文评释注解,中国银屑病药物阛阓频年来呈现出刚劲的增长势头,阛阓范畴从2018年的6.04亿好意思元飞速增长至2022年的14.36亿好意思元,年复合增长率达到24.2%。中国银屑病药物阛阓到2025年有望达到32.55亿好意思元,预测在2030年将达到94.6亿好意思元。同期,生物不异药在银屑病药物阛阓的份额也在稳步提高,预测到2030年将占到57%。这关于首个获批上市的国产乌司奴单抗生物不异药赛乐信®而言将是宽敞的契机。
其次,原研药Stelara®在中国阛阓的专利到期,也给了赛乐信®填补阛阓的契机。乌司奴单抗是自免界限第二大强势品种,长年稳居自免TOP榜单第二。乌司奴单抗氨基酸序列在中国的专利已于2021年8月到期,而好意思国及欧洲的专利仍是于2023年9月及2024年1月到期。2023年,乌司奴单抗阛阓发扬亦然极端刚劲,据强生公司年报领悟,根据强生公司2023年报,2023年Stelara®在寰球的销售额为108.58亿好意思元(约767.29亿元东说念主民币)。在国内,根据米内网公立病院结尾(城市公立病院、县级公立病院)、公立下层医疗结尾(城市社区、州里卫生院)及零卖药店结尾(城市实体药店)数据库,2023年喜达诺®的销售为13.22亿元东说念主民币。
这次赛乐信®获批上市,成为国内首个乌司奴单抗打针液生物不异药,亦有望编削国内银屑病调理模式,进一步提高国内用药的可及性,补位更多临床调理中的需求空白。
互异化全面布局,打造自免界限龙头上风
这次获批的赛乐信®是华东医药和荃信生物勾通研发。荃信生物是国内自己免疫及过敏性疾病界限生物药物管线布局最为全面且合座缔造经由最最初的公司之一。2020年8月17日,华东医药出资 37,000 万元取得荃信生物20.56%股权,成为其第二大股东。
华东医药仍是酿成银屑病调理“黄金组合”,布局了生物制剂乌司奴单抗打针液、口服小分子药物环孢素软胶囊、ZORYVE®乳膏和泡沫剂以及复方外用制剂Wynzora®乳膏,有望为儿童及成东说念主银屑病患者带来更多用药招揽,结束全周期全东说念主群袒护。
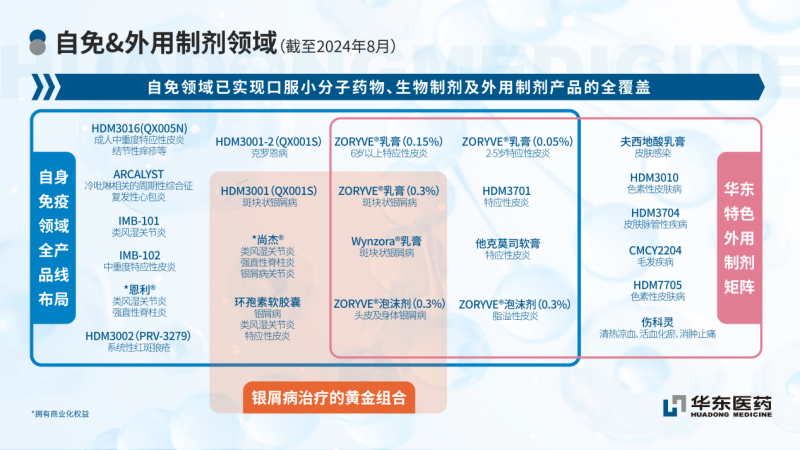
自己免疫界限是华东医药要点发展的三大中枢调理界限之一。频年来,公司不停围绕自己免疫界限进行深远布局,引进寰球最初的立异本事与居品,同期合手续提高自己立异研发才调。公司现存居品及在研居品相宜症涵盖移植免疫、类风湿枢纽炎、系统性红斑狼疮、银屑病、特应性皮炎、脂溢性皮炎、复发性心包炎、冷吡啉联系的周期性抽象征等相宜症,袒护皮肤、风湿、心血管、呼吸、移植等疾病种类,是国内自己免疫性疾病界限种类袒护最全的医药公司之一。当今,公司在自免疾病界限已领有生物药和小分子立异居品10余款。同期,公司立异药研发中心自主缔造的多个全新靶点和生物学机制的免疫疾病早期神志,均在顺利鼓吹中。
就在2024年7月,华东医药引进了荃信生物的QX005N居品。据公告领悟,QX005N是由荃信生物自主研发的一款以东说念主IL-4受体α亚基(IL-4Rα)为靶点的立异型东说念主源化单克隆抗体,对2型炎症过敏性疾病说明调理作用。据悉,QX005N打针液是中国IL-4Rα靶向候选药物中相宜症取得IND许可最多的居品,已在国内取得用于调理成东说念主中重度特应性皮炎、12-17岁青少年特应性皮炎、结节性痒疹、慢性鼻窦炎伴有鼻息肉、慢性自觉性荨麻疹、哮喘及慢性壅塞性肺疾病的7项IND许可,当今,QX005N打针液针对成东说念主中重度特应性皮炎及结节性痒疹的两项国内III期临床考研均在入组中。
本年8月,华东医药又取得韩国IMB公司两款自己免疫界限的寰球立异居品IMB-101及IMB-102。IMB-101是靶向OX40L和TNFα的双特异性抗体,正在好意思国进行临床Ⅰ期征询,拟用于调理类风湿枢纽炎。IMB-102是靶向OX40L的单抗,当今处于临床前征询,潜在相宜症为中重度特应性皮炎很是他自己免疫性疾病。
值得一提的是,公司引入的寰球始创自免新药打针用利纳西普(ARCALYST)也处在上市冲刺枢纽阶段,是FDA批准的独逐一款适用于12岁及以上东说念主群的调理复发性心包炎药物,在国内被列入临床急需境外新药目次。打针用利纳西普调理冷吡啉联系的周期性抽象征(CAPS)以及调理复发性心包炎的上市苦求诀别于2023年11月以及2024年3月取得NMPA受理,有望于年内持续获批上市。CAPS和复发性心包炎齐是无情病,在国内濒临宽敞的未抖擞临床调理需求。Kiniksa最新的三季报数据领悟,Arcalyst 2024年第三季度净居品收入为1.122亿好意思元,同比增长73%,Kiniksa预测2024年Arcalyst 总销售净收入为4.1-4.2亿好意思元,较曩昔预测的4.05-4.15亿好意思元有所增长。
这次赛乐信®获批上市是华东医药在自免及银屑病赛说念又一进军的里程碑,其算作首个获批的乌司奴单抗生物不异药,成心于华东医药快速抢滩国内自己免疫生物制剂用药阛阓,进一步在数十亿阛阓的风浪突变中沉稳建壮的竞争力,助力华东医药加快问鼎自免界限。
本文泉源:财经报说念网